
 顶级伦理片
顶级伦理片

中枢撮要:
1. 中国国度医保局近期晓示,暂停入口印度瑞迪博士实验室进入中国集采的仿制药物盐酸托莫西汀胶囊。这家涉事的仿制药企业在印度排行第3,全球排行前10。这一仿制药爆雷事件,激发东说念主们对中标仿制药的灵验性和安全性的担忧。
2. 据国度卫健委数据,在当今4000多家中国制药企业中,90%以上是仿制药企业。宇宙17万药品批文中,95%以上亦然仿制药。中国这些年来一径直力于于进行仿制药质地和疗效的评价,不停细化评价模式、参比制剂、临床考试等方面实际,继承一致性评价措施,以普及仿制药质地。
3. 在制药界,一个无法幸免的话题是集采,即药品的聚合带量采购。带量集采但愿达到三个方针:药价低、药效高、药物的供应量饱和。然而,当经济周期进入下行轨说念,人人都面对降本增效的时候,如果价钱是最环节的方针,就不可幸免会有“偷工减料”发生,大肆资本带来的是药物养息成果的裁汰,以及药物的质地问题。唯独着实被老匹夫招供、灵验,仿制药才会成为好药。要达到这几个场地,仿制药还有很长的路要走。
作家丨张洪涛 网《CC谍报局》特约撰稿员
裁剪丨白金娜、黄舒琪、王俊豪

印度仿制药再爆雷?
商讨标明,一款进入中国的印度仿制药“未达到应有的血药浓度”
8月30日,中国国度医保局晓示印度瑞迪博士实验室进入集采的仿制药物盐酸托莫西汀胶囊,在原料药、工艺考据、质地放胆等方面存在劣势,对该居品继承暂停入口、销售和使用措施!
盐 酸托莫西汀是第一个被FDA批准用于养息多动症的药物, 由于中国药品集采的价钱竞争,礼来的原研居品已于本年1月在中国罢手供应。 也即是说, 这款原研入口药已无法在病院买到。

这家出事的印度 瑞迪博士实验室是印度排行第三的仿制药企业, 全球排行前十。这一仿制药爆雷事件,激发东说念主们对中标仿制药的灵验性和安全性的担忧。
就在处罚令下达不久,这家印度公司旗下的另一款神经病仿制药奥氮平 再爆出现了“未达到血药浓度”的问题。

奥氮平是第一个获准用于养息急性双相躁狂症的非典型抗神经病药物,原研厂家为礼来 。奥氮平的中国首仿是江苏豪森,于2001 年上市,是宇宙首家通过一致性评价, 商场占有率60%以上的氮安平仿制药。2019年,堪称“价钱屠户”的印度迪瑞旗下的仿制药奥氮平片(奥兰之),以超廉价钱6.19元/片价钱中标。 而上一轮“4+7”中,豪森药业的中标价为9.64元/片。
印度版氮安平中标,意味着中国联系病院,要从之前的仿制药再调理到新的中标仿制药,这两种仿制药之间的养息成果是否一致,这些药物是否与原研品牌药一样安全灵验?
由湘雅二院国度精神防碍临床商讨中心、宁波康宁病院进行的一项商讨标明,在30名患者中,从集采前的氮安平仿制药调理到中标的印度仿制药之后,扫尾显现印度迪瑞的这款中标仿制药奥氮平的“血药浓度权贵低于另一款中国仿制药。”
同期标明,两种仿制药之间“可能不具有养息等效性或生物等效性。每次调理都可能酿成疗效或耐受性的变化。”

这篇商讨发表于《药理学前沿》。这项商讨天然标明,“在换药前后莫得权贵各别。”
但血药浓度不够顶级伦理片,对于一款药物的养息成果,可能是一个严重的潜在问题!
实 际上, 能否达到药物的灵验浓度,是一款药物能否达到理念念药效的环节!
药物血浆浓度与药品的临床诈欺密切联系。许多疾病常常都会对所服用的药物有明确数值的血药浓度模式。唯独血药浓度达到灵验浓度智力显效,浓度越高成果越强,但如超出了安全领域则可显现出毒性反馈。

这篇论文的商讨者冷落, 患者在两个仿制药之间调理时,可能需要对疗效或耐受性的变化进行检测。 商讨者还同期冷落药企应清晰系数上市仿制药和品牌药的药理等效性和生物等效性数据,并制定后续临床样本养息等效性评估和养息不等效性监测智商的指示原则。


为何要对2007年10月之前的仿制药进行一致性评价?
仿制药之间都有各别,那么仿制药和原研药之间是否有更大的各别呢?
在一篇最近激发世俗争议的自媒体著述的著述中(“好多入口药,悄无声气的隐没了”),发扬了一个杭州家长得了支原体感染,开不到入口药,唯独国产打针型阿奇霉素,养息成果不好,后终于用上了入口药物,孩子的高烧本日就退了下来。
天然这可能仅是个案,但不仅是浅显的耗尽者对仿制药的质地忧心忡忡,医务东说念主员同样有这么的记念。
《健康计谋》上发表过一篇对于“大夫对仿制药的办法”的走访答复,走访时候为2020 年,走访领域是宇宙各地的医师,共有598东说念主参与走访。其中,仅有 35.8%的东说念主以为仿制药与原研药有同等养息成果, 36.5%的东说念主以为仿制药和原研药的安全性一致。唯唯一半的东说念主(49.2%)得志给我方的病东说念主或家东说念主使用仿制药,而 45%的东说念主更得志推选使用原研入口药,即便其价钱更高。[2]
据卫健委的数据,当今4000多家中国制药企业中,90%以上都是仿制药企业。宇宙17万药品批文中,95%以上都是仿制药。
1314酒色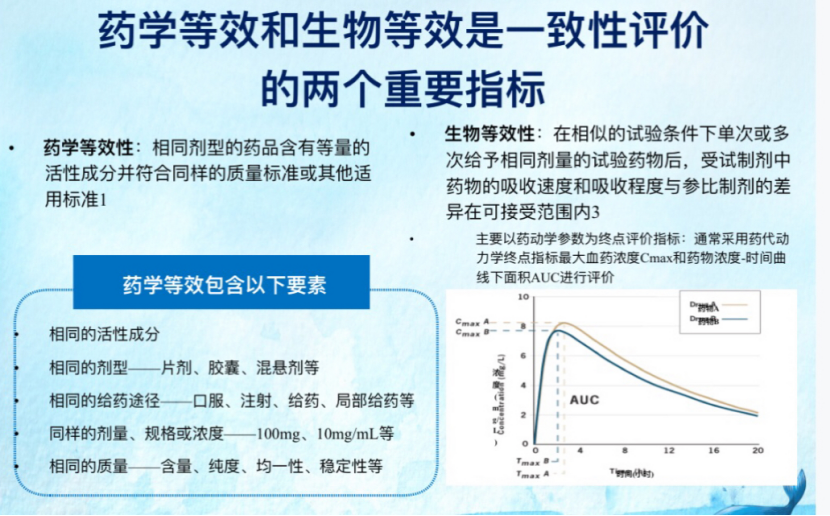
仿制药的质地行弗成?要回复这个问题,需要的不是标语,而是轨范化的审批历程及监管。
因为历史性的原因,也因为中国的当代制药时间之前不够先进,仿制药的水平是错杂不皆的,致使有频繁包含假冒伪劣药品。针对这个问题,中国驱动全面执行实施“仿制药一致性评价”,在2002年,《药品管制法实施条例》奏效,仿制药的审核模式获得调和。2007年,药监局律例仿制药应在五个方面与原研品牌药保抓一致:(1)活性要素;(2)给药道路;(3)剂型;(4)规格;(5)养息成果。
2012年至2018年,先后三次颁发文献,条目对2007年10月1日前批准上市的化学药品仿制药口服固体制剂完成一致性评价,期限为2018年年底前。所触及的仿制药品品种为289个。
可见,中国这些年来一径直力于于进行仿制药质地和疗效的评价,不停细化评价模式、参比制剂、临床考试等方面实际,以普及仿制药的养息。当今中国通过一致性评价(包括视同通过)的受理号已逾越7000个,触及药品逾越1000个。
然而,一致性评价要与原研药作念对比,由于原研药的价钱有各别,不同药物的一致性评价资本也就不可能相似。然而不错看出,作念一个一次性评价,至少需要数百万元的过问。
一致性评价这个措施,增多了药物的资本,但普及了仿制药的质地。

▎仿制药一致性评价象征

数十家有名跨国药企与中国仿制药企,因药品性量等问题,被罢手集采中选经历
在制药界,一个无法幸免的话题,是药品的聚合带量采购,简称集采。
天然,集采并不是中国的特质,在2024年,好意思国也驱动了集采。所不同的是,好意思国集采的品种,主如若还是上市多年的药物,而在中国,集采的不单是是仿制药,还包括了刚上市不久的立异药。

集采的一个方针,是把药价打下来。 在中国,这个成果口舌常明显的,多家药品坐蓐企业参与集采竞标,其实亦然在打价钱战。进入集采的药物,价钱都会腰斩,致使膝斩。
数据标明,进入“4+7”集采之后,中标的原研药和仿制药日均用度辩认减少了44.44%和79.00%,莫得进入集采的原研药也感受到了压力,日均用度减少了15.10%。【3】
然而打压药价,并非是唯一的方针。事实上,至少在中国,带量集采但愿达到三个方针:药价低、药效高、药物的供应量饱和。

为了保证药效高,集采条目中选药品必须通过一致性评价,确保与原研药在质地和疗效上一致。同期,联系部门还会加强全历程质地监管和抽检频次,对非法违法企业进行追责。
在中标品种的价钱基础上,会制定出医保支付模式,从而调换医疗机构和患者形成合理的用药习气,从需求端来刺激药品的坐蓐,饱读舞药企提供饱和的药物。
对于一些家底比拟殷实的制药企业,集采有助于他们本就念念伸开的价钱战,挤掉一些体量比拟小的竞争者。然而,当经济周期进入下行轨说念,人人都面对降本增效的时候, 如果价钱是最环节的方针,就不可幸免会有“偷工减料”发生。
坐蓐奥氮平片的印度瑞迪博士实验室,其以“价钱屠户”著称, 以超低的价钱击败之前进入集采的国产仿制药与原研药,但其价低同期并莫得保证药物资量, 本年8月底,国度医保局暂停了瑞迪博士实验室参与国度集采的禀赋,而此前印度排行第一的太阳制药也因仿药质地问题,被中国取消集采中选经历。印度是全球最大的仿制药坐蓐国, 但数据作秀、管制疏漏、资本压缩等问题长久未能措置。

而据统计,包括韩国大熊制药的打针用头孢地嗪钠、葛兰素史克公司(GSK)度他雄胺胶囊、优时比公司的抗癫痫药左乙拉西坦打针用浓溶液等,先后因药物微生物混浊、质地问题等,被取消集采中选经历。
仿制药并非中国特质。稀有据显现,2015 年好意思国商场上 89%的药物是仿制药,其中大部分来自印度。据《仿制药的真相》一书清晰:“为裁汰资本,在司理的授意下,公司的科学家们将高纯度要素替换成低纯度要素,以大肆资本。”
大肆资本带来的是药物养息成果的裁汰,以及药物的质地问题。
因为无法承受价钱的压力,一些入口原研药澌灭竞标,致使退出了中国商场。与此同期,在入口药悄无声气地隐没的时候,一些中标的集采药也隐没了。
据媒体不统统统计,唯独161种入口药未在中国再注册,其中不乏昔时临床常用的有名药品。
这可能即是咱们很难在病院买到入口原研药的原因之一了吧!
但对老匹夫来说,评价药物蛮横,不看告白,看疗效!
唯独仿制药着实被老匹夫招供,灵验,仿制药才会成为好药!
但这一天,算计仍有漫长的路要走。

1.Zhang C, Ding Y, Wu Z, Wang J, Wu X, Xie W. Does China's competitive generic substitution policy deliver equivalent clinical outcomes? A pilot study with two generic formulations of olanzepine. Front Pharmacol. 2023 Feb 22;14:1097600.
2.He J-H, et al. Physicians’ perceptions of generic drugs in China. Health Policy OPEN, Volume 3. 2022, 100067
3.Wang J, Yang Y, Xu L, et al. Impact of “4+7” volume-based drug procurement on the use of policy-related original and generic drugs: a natural experimental study in China. BMJ Open 2022;12:e054346. doi: 10.1136/bmjopen-2021-054346
